Good Engineering Practice GMP-Aufwand für Qualifizierungsdokumentation wird häufig unterschätzt
Die Vorgaben der Good Manufacturing Practice (GMP) anzuwenden, gehört für den Maschinenbau in der Medizintechnik- und Pharmabranche zu den wichtigsten Grundsätzen. Neben der technischen Anlagendokumentation ist auch die erweiterte GMP-konforme Qualifizierungsdokumentation umzusetzen – eine Aufgabe, die nicht gerade zum Kerngeschäft der meisten Maschinenbauer gehört und daher gern auf die lange Bank geschoben wird.
Anbieter zum Thema
„Der Aufwand einer pharmagerechten Dokumentation wird häufig nicht richtig eingeschätzt“, weiß Simone Kuhn zu berichten. Sie verantwortet den Bereich GMP-Systeme bei Contexo in Winterbach, einem Spezialisten für individuelle Automatisierungslösungen, der bereits seit vielen Jahren gefragter Partner erfolgreicher Medizintechnikhersteller ist.
GMP-Richtlinien ohne Gesetzes-Charakter
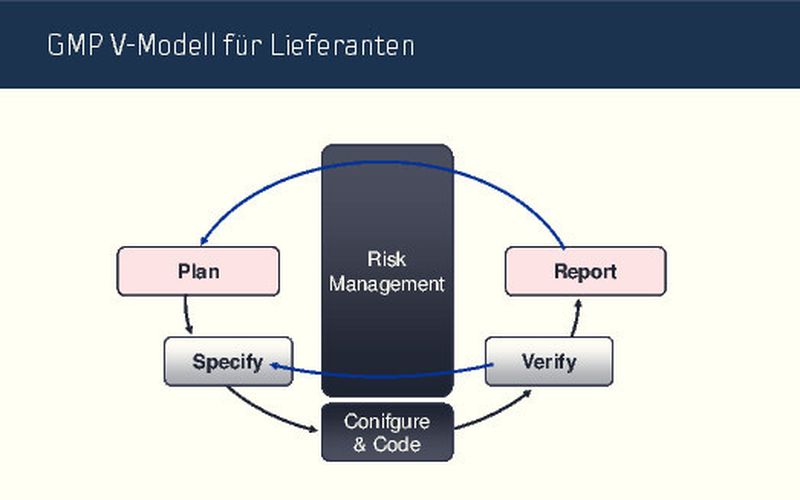
Das Problem: Die Richtlinien besitzen keinen Gesetzes-Charakter für Lieferanten. Bei dem Verfahren kann man sich also nicht auf klar definierte Grundlagen stützen, dementsprechend groß ist der Ermessensspielraum. Die Vorstellungen, wie dieser auszulegen ist, gehen oft weit auseinander. Drei Grundbedingungen müssen jedoch auf jeden Fall erfüllt sein:
- risikobasierte Vorgehensweise,
- GMP-gerechte Dokumentationserstellung
- Rückverfolgbarkeit.
„Gesunder Menschenverstand statt blindem Aktionismus spielt hierbei eine entscheidende Rolle“, unterstreicht Kuhn. Durch begleitendes Engineering und risikobasierte Vorgehensweise sei der Dokumentationsaufwand auf ein angemessenes Maß zu bringen.
GMP-Unterstützung und Rundum-sorglos-Pakete
Das Angebotsspektrum reicht bei Contexo von der beratenden Unterstützung bis zum Rundum-sorglos-Paket, das die komplette Dokumentation mit den erforderlichen Spezifikationen, der Protokollerstellung, Testdurchführungen und Ergebnisdokumentation umfasst. Für einen mittelständischen Verpackungsmaschinen-Hersteller erstellt Contexo beispielsweise die erweiterte GMP-Dokumentation mit Designdokumenten (FDS, HDS, SDS), Installationsqualifizierung (IQ) und Funktionsqualifizierung (OQ). „Wichtig ist, dass wir als Dienstleister schon während der Auftragserteilung mit im Boot sitzen“, betont Kuhn. Die GMP-Dokumentation müsse immer ein begleitendes Projekt sein.
(ID:35153590)





:quality(80)/p7i.vogel.de/wcms/2e/f2/2ef22b4819105332e99956027e9f71a9/0131117278v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/86/dc8605158dce64ebe28e103b890f945a/0131059658v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/43/964337b0e2469e4506e124daea12a645/0130932880v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/c4/b9/c4b9fbf1fd89c205038c4b8b654672fb/0130996736v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ea/bd/eabdfc2a66aff16e6d63dd49f161519e/0131142465v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/68/72/687281badac9e82f30f89a22c2eaf22a/0131063729v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/de/fa/default_article/default-article-image.jpeg)
:quality(80)/p7i.vogel.de/wcms/85/c7/85c74a0eef2af1053ee28c0d4a5c1dcb/0131008766v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/6f/c1/6fc119c5fd8ee719b634ce7fa47e8d73/0131139737v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/97/6c/976cb834c8896270728c1ddbb4dbfc97/0131123269v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/16/d3/16d3e08f9404aae1cec19cf11f471e27/0126703504v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/eb/ab/ebabc3a0cbf070ead54f932bbfed7efb/0130987887v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/1f/dc/1fdccc5707da698efe0cd92be64e8206/0131003288v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/07/44/0744241eca00864cdb0aedb88d025a2b/0130969280v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/f3/51/f3517786ccc07ed00107e2d75a982c1b/0131011686v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/c8/70/c870817ce104356eb4103b36c7116a04/0130902111v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/99/5c/995ce67e5f21e175bad70103ac9911b9/0130784835v2.jpeg)
:fill(fff,0)/p7i.vogel.de/companies/60/35/60353b32617d5/logo-kumavision-400x100px.png)
:fill(fff,0)/p7i.vogel.de/companies/66/9f/669f70597f87e/consense-logo-qm-500-x-500.png)
:fill(fff,0)/p7i.vogel.de/companies/5f/b6/5fb69cb5dff5e/metecon-logo-rgb-300dpi.jpg)
:quality(80)/p7i.vogel.de/wcms/00/92/0092acd5ff4cd981c40b0a5f1287f1e9/0124963932v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/8a/3b/8a3b4ac8ae9a5498dd4881f0eaa46fae/0126772696v2.jpeg)