Consense Software-Validierung nach GAMP 5: im Komplettpaket zur Freigabe
Zur Gewährleistung der Produktqualität müssen Medizintechnikhersteller ein systematisches und zuverlässiges Qualitätssicherungssystem vorweisen. Softwaregestützte Managementsysteme sind für viele zum elementaren Bestandteil des Qualitätssicherungssystems geworden.
Anbieter zum Thema
- Software für die Anforderungen der „Guten Arbeitspraxis“ (GxP)
- Software-Validierung als dokumentierter Nachweis der Erzielung und Erhaltung der Konformität mit anzuwendenden GxP-Vorschriften
- Vorgaben durch Annex 11 der EudraLex Vol. 4 GMP Richtlinie, FDA 21 CFR Part 820.70 und FDA Title 21 CFR Part 11 sowie ISO 13485:2016.
Allein die zu planenden, durchzuführenden und zu dokumentierenden Qualifizierungen und Validierungen bedeuten für diese Unternehmen einen immensen Arbeitsaufwand. Die Consense GmbH, Softwareentwickler und Dienstleister rund um Qualitäts- und Integrierte Managementsysteme, hat die Software Consense GxP entwickelt, die auf die Anforderungen der „Guten Arbeitspraxis“ (GxP) zugeschnitten ist. Ist der Einsatz einer solchen Software in Herstellungs- und Qualitätssicherungsprozessen, deren Arbeitsergebnisse sich auf die Qualität des Endprodukts negativ auswirken können, geplant, so gibt es auch dazu Vorgaben aus diversen Regelwerken. Einige Beispiele sind Annex 11 der EudraLex Vol. 4 GMP Richtlinie, die US-amerikanische Richtlinie FDA 21 CFR Part 820.70 und FDA Title 21 CFR Part 11 oder die ISO-Norm 13485:2016.
Vor dem Einsatz der Software ist eine Software-Validierung vorgeschrieben. Darunter versteht man den dokumentierten Nachweis der Erzielung und Erhaltung der Konformität mit anzuwendenden GxP-Vorschriften (wie GMP, GDP, GCP, GAMP) sowie den dokumentierten Nachweis der Eignung der Software. Die Eignung bezieht sich auf den vorgesehenen Einsatzzweck und wird bemessen an der reproduzierbaren Erfüllung der vorab spezifizierten Anforderungen im praktischen Einsatz. Vereinfacht ausgedrückt: Es muss belegt werden, dass die Software das leistet, was sie leisten soll.
Aufgrund der komplexen Vorgaben sollte bereits bei der Auswahl einer geeigneten Software darauf geachtet werden, dass diese nach hohen Qualitätsstandards, beispielsweise gemäß ISO 9001, entwickelt wurde. Eine Standardsoftware wie Consense GxP ist zu bevorzugen, da Validierungsumfang und -tiefe geringer sind als beim Einsatz kundenspezifischer Software. Consense GxP wird darüber hinaus bereits unter Berücksichtigung der vorgesehenen Validierung entwickelt und vorvalidiert ausgeliefert.
Die sorgfältige Auswahl der Software beeinflusst den Validierungsaufwand
Eine Software-Validierung orientiert sich häufig am international anerkannten Leitfaden „GAMP 5 – Ein risikobasierter Ansatz für konforme GxP-computergestützte Systeme“ der International Society for Pharmaceutical Engineering (ISPE). GAMP steht für „Good Automated Manufacturing Practice“.
Consense hat in Anlehnung an die GAMP 5-Vorgehensweisen bereits zahlreiche Validierungen ihrer Software Consense GxP in der Betriebsumgebung von Kundenunternehmen beratend und mitwirkend begleitet. Dem Rahmenwerk GAMP 5 folgend, wird die Software in einem solchen Validierungsprojekt auf Basis zuvor aufgestellter Anforderungskriterien in der später verwendeten Umgebung installiert, geprüft und nach erfolgreichem Abschluss freigegeben. Dabei ist entscheidend, dass sich die Validierung auf den tatsächlichen Einsatz der Software im konkreten Prozess bzw. Betriebsumfeld konzentriert. Die Prüfung erfolgt anhand von Testszenarien, welche die zuvor definierten Anforderungskriterien enthalten. Die Tests sollen nicht nur die reine Systemfunktionalität belegen, sondern den Einsatz der Software in der Betriebsumgebung bzw. im konkreten Prozess inklusive der dazugehörigen Risiken nach messbaren Kriterien prüfen. Somit sollen möglichst alle relevanten Anwendungsfälle und Risikopotenziale, die mit dem Einsatz der Software verbunden sind, abgedeckt und beherrschbar gemacht werden.
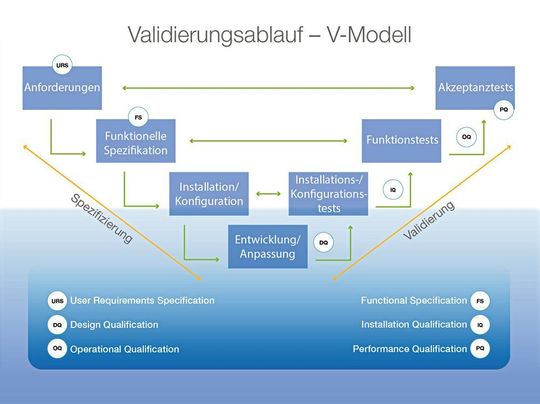
Das Vorgehen folgt dabei dem V-Modell, welches die Validierung in mehreren Projektphasen organisiert. Jede der Projektphasen wird durch eine detaillierte Dokumentation begleitet. Bei dieser Dokumentation im Rahmen der Software-Validierung bietet die Consense GmbH qualifizierte Beratung und mitwirkende Unterstützung im Komplettpaket mit der vorvalidierten Standardsoftware Consense GxP.
Ziel der Software-Validierung ist der Nachweis, dass der Output beim vorgesehenen Einsatzzweck wie erwartet und reproduzierbar ist und somit die vorher definierten Anforderungen erfüllt wurden. Dies muss am Ende ganz klar zu bewerten sein, um zu entscheiden, ob die Software in der beabsichtigten Weise für die GxP-relevanten Prozesse eingesetzt werden darf. Der Validierungsbericht dient dabei als „Antwort“ auf den Validierungsplan: Er beschreibt abschließend alle Validierungstätigkeiten. Mit der Freigabe des Validierungsberichts erhält die Software die Genehmigung für den produktiven Betrieb unter GxP-Bedingungen.
Einerseits bedeuten die umfassenden Vorgaben hohe Aufwände für die regulierten Unternehmen – gleichzeitig bringen sie aber auch einen geschäftlichen Nutzen: Denn gut definierte und spezifizierte Systeme sind leichter zu pflegen, haben kürzere Ausfallzeiten und führen zu geringeren Betriebs- und Instandhaltungskosten. Zudem werden Fehler häufig früher erkannt und die kontinuierliche Verbesserung vorangetrieben.
Lesen Sie auch:
:quality(80)/images.vogel.de/vogelonline/bdb/1604200/1604253/original.jpg)
Transline
Klarheit in jeder Sprache – Compliance bei der Übersetzung von Labels
:quality(80)/images.vogel.de/vogelonline/bdb/1387100/1387183/original.jpg)
Grundlagenwissen
Qualitätsmanagement in der Medizintechnik: Definitionen, Ziele und Tools
Weitere Artikel zu Management-Themen finden Sie in unserem Themenkanal Management.
(ID:46102534)





:quality(80)/p7i.vogel.de/wcms/6f/ba/6fba23516c929940033f16878d9806a0/0131167864v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/2e/f2/2ef22b4819105332e99956027e9f71a9/0131117278v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/86/dc8605158dce64ebe28e103b890f945a/0131059658v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/43/964337b0e2469e4506e124daea12a645/0130932880v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ea/bd/eabdfc2a66aff16e6d63dd49f161519e/0131142465v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/68/72/687281badac9e82f30f89a22c2eaf22a/0131063729v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/de/fa/default_article/default-article-image.jpeg)
:quality(80)/p7i.vogel.de/wcms/85/c7/85c74a0eef2af1053ee28c0d4a5c1dcb/0131008766v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/6f/c1/6fc119c5fd8ee719b634ce7fa47e8d73/0131139737v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/97/6c/976cb834c8896270728c1ddbb4dbfc97/0131123269v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/16/d3/16d3e08f9404aae1cec19cf11f471e27/0126703504v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/eb/ab/ebabc3a0cbf070ead54f932bbfed7efb/0130987887v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/25/d0/25d0637502c1a8591a6aa5b32b330d57/0131173181v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/07/44/0744241eca00864cdb0aedb88d025a2b/0130969280v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/f3/51/f3517786ccc07ed00107e2d75a982c1b/0131011686v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/c8/70/c870817ce104356eb4103b36c7116a04/0130902111v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/99/5c/995ce67e5f21e175bad70103ac9911b9/0130784835v2.jpeg)
:fill(fff,0)/p7i.vogel.de/companies/66/9f/669f70597f87e/consense-logo-qm-500-x-500.png)
:fill(fff,0)/p7i.vogel.de/companies/60/35/60353b32617d5/logo-kumavision-400x100px.png)
:fill(fff,0)/p7i.vogel.de/companies/68/ec/68ecbe6adfb73/aptean-logo---black.jpeg)
:quality(80)/p7i.vogel.de/wcms/b2/7e/b27e531f64e68d2cbd4f95f7be8da781/0129731819v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/8a/3b/8a3b4ac8ae9a5498dd4881f0eaa46fae/0126772696v2.jpeg)