Technische Universität München Neue 3D-Drucktechnik für Scaffolds zur Wiederherstellung von Knorpel
Eine neue internationale Forschungsarbeit hat sich mit der Wiederherstellung von Knorpel befasst – eine schwierige Aufgabe, denn Knorpel muss elastisch, aber auch mechanisch belastbar sein. Die Forscher untersuchten dafür eine neue Kombination von Mikrofaser-Gerüsten aus dem 3D-Drucker und Hydrogelen.
Anbieter zum Thema
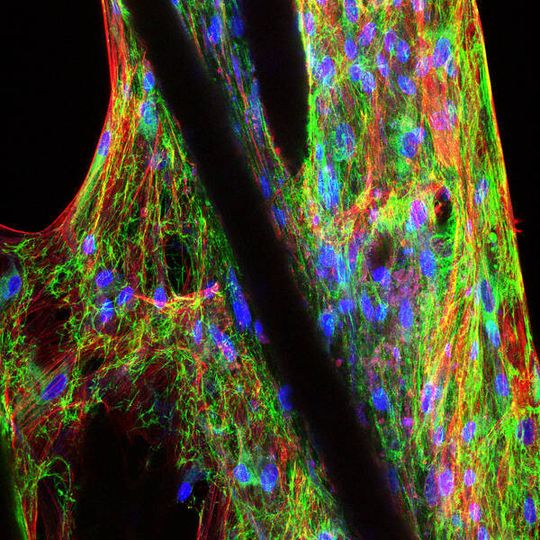
In solchen sogenannten Scaffolds können menschliche Knorpelzellen wachsen, sodass neues Knorpelgewebe entsteht. Die für die Studie untersuchten Materialkombinationen zeigen eine zu Kniegelenks-Knorpelgewebe vergleichbare Elastizität und Steifigkeit. Zudem unterstützten sie das Wachstum und die Vernetzung menschlicher Gewebezellen. Die Wissenschaftler der Technischen Universität München (TUM) erwarten, dass sich dieser neue Ansatz auch auf andere Forschungsfelder im Bereich Soft-Tissue-Engineering auswirken wird, beispielsweise auf die Rekonstruktion von Brustgewebe und die Herstellung von Herzgewebe. Die Ergebnisse wurden nun in der Zeitschrift Nature Communications veröffentlicht.
Was verbirgt sich hinter Melt Electrospinning Writing?
Eine Schlüsselrolle spielt dabei eine neue 3D-Drucktechnik, das sogenannte Melt Electrospinning Writing. Sie ermöglicht die Herstellung von Strukturen, die gleichzeitig genügend Raum für Zellwachstum bieten, aber auch die benötigte mechanische Steifigkeit gewährleisten. „Melt Electrospinning Writing bietet mehr Freiheit bei der Gestaltung von Gerüsten und begünstigt so die Heilung und das Wachstum von neuem Gewebe“, erklärt Prof. Dietmar W. Hutmacher, einer der Hauptautoren der Veröffentlichung. „Sie ermöglicht uns, die Art und Weise, wie die Natur Gelenkknorpel baut, genauer nachzuahmen“, erklärt er, „das heißt, wir verstärken ein weiches Gel – Proteoglykane oder, wie in unserem Fall, ein biokompatibles Hydrogel – mit einem Netz aus sehr dünnen Fasern.” Die mit Hilfe von Electrospinning Writing hergestellten Gerüstfasern können bis zu 5 µm im Durchmesser dünn sein. Gegenüber herkömmlichen Methoden sind die Fasern damit 20-mal dünner.
Hydrogel-Faserverbundwerkstoffe herstellen
Prof. Hutmacher forscht an der Queensland University of Technology in Australien und arbeitet derzeit als Hans Fischer Senior Fellow am TUM Institute for Advanced Study. Gastgeber für seine TUM-IAS Focus Group für regenerative Medizin ist TUM-Prof. Arndt Schilling, Leiter der Forschungsabteilung für Plastische Chirurgie und Handchirurgie an der Universitätsklinik Klinikum rechts der Isar.
An der Arbeit waren Forscher aus Australien, Deutschland, den Niederlanden und dem Vereinigten Königreich beteiligt, so dass für die Untersuchung ein breites Spektrum an Forschungswerkzeugen eingesetzt wurde. Die Hauptarbeit konzentrierte sich auf die Entwicklung, Herstellung und mechanische Prüfung der Hydrogel-Faserverbundwerkstoffe. Ergänzend wurden Vergleiche mit Kniegelenkknorpel von Pferden, Experimente mit dem Wachstum von menschlichen Knorpelzellen in der künstlichen Matrix und Computersimulationen durchgeführt.
Die Ergebnisse legen einen Durchbruch nahe
Alle Ergebnisse deuten auf einen – von Prof. Hutmacher noch vorsichtig formulierten – Durchbruch hin. Nachdem die Forscher das Computermodell der Hydrogel-Faserverbundwerkstoffe validiert hatten, nutzen sie es nun, um eine Vielzahl unterschiedlicher Anwendungsmöglichkeiten zu beurteilen. „Das neue Verfahren ist nicht nur für die Reparatur von Gelenken vielversprechend, sondern auch für Anwendungen wie zum Beispiel die Rekonstruktion der Brust nach einer Amputation im Zug einer Krebstherapie oder für die Züchtung von Herzgewebe“, sagt Prof. Hutmacher. „Wir müssen das Gerüst unter den Muskel implantieren und unser neues faserverstärktes Hydrogel könnte sich dabei als entscheidend erweisen für die Regeneration sowohl von großen Mengen an Brustgewebe als auch von biodynamisch stark belasteten Herzklappen.“
Prof. Hutmacher und seine Kollegen an der TU München – Prof. Arndt Schilling, PD. Dr. Jan-Thorsten Schantz, und Dr. Elizabeth Balmayor – planen bereits, die in Nature Communications beschriebene Herangehensweise für ihre Forschungen zu Tissue Engineering von Brustgewebe einzusetzen. Außerdem haben sie zusammen mit der Gruppe von Prof. Stefan Jockenhövel und Dr. Petula Mela an der RWTH Aachen ein Projekt zur Herstellung von Herzklappengewebe begonnen.
Gefördert wurden die Forschungsarbeiten von der Europäischen Kommission, dem EU Forschungsrahmenprogramm FP7, der niederländischen Regierung, der niederländischen Arthritis Stiftung, und dem Nationalen Forschungsrat für Gesundheitswesen und Medizin in Australien. Das TUM IAS wird unterstützt durch die deutsche Exzellenzinitiative und das EU Forschungsprogramm FP7.
(ID:43387576)





:quality(80)/p7i.vogel.de/wcms/2e/f2/2ef22b4819105332e99956027e9f71a9/0131117278v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/dc/86/dc8605158dce64ebe28e103b890f945a/0131059658v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/96/43/964337b0e2469e4506e124daea12a645/0130932880v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/c4/b9/c4b9fbf1fd89c205038c4b8b654672fb/0130996736v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/68/72/687281badac9e82f30f89a22c2eaf22a/0131063729v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/de/fa/default_article/default-article-image.jpeg)
:quality(80)/p7i.vogel.de/wcms/85/c7/85c74a0eef2af1053ee28c0d4a5c1dcb/0131008766v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/16/d3/16d3e08f9404aae1cec19cf11f471e27/0126703504v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/97/6c/976cb834c8896270728c1ddbb4dbfc97/0131123269v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/eb/ab/ebabc3a0cbf070ead54f932bbfed7efb/0130987887v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ab/6e/ab6e66f6ff5fb536bbb5f2a69308dda1/0130948875v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/1f/dc/1fdccc5707da698efe0cd92be64e8206/0131003288v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/35/8d/358d5b626ee5c1aafce1c6afc271a29b/0130820430v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/07/44/0744241eca00864cdb0aedb88d025a2b/0130969280v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/48/3f/483ff135ac1fad514855aa37fa4715a3/0130860797v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/f3/51/f3517786ccc07ed00107e2d75a982c1b/0131011686v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/c8/70/c870817ce104356eb4103b36c7116a04/0130902111v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/99/5c/995ce67e5f21e175bad70103ac9911b9/0130784835v2.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/130700/130777/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/5f/b6/5fb69cb5dff5e/metecon-logo-rgb-300dpi.jpg)
:fill(fff,0)/p7i.vogel.de/companies/5d/f8/5df8ac8a157ae/logo.png)
:quality(80)/p7i.vogel.de/wcms/94/8b/948b28e3e307c87f8b51b15abeb6d6a5/0126154746v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/c6/df/c6dfa446dd927dcc4732db623887912d/0129791016v2.jpeg)